1.离子键理论
活泼金属原子与活泼的非金属原子所形成的化合物,如NaCl,KCl等,通常都是离子型化合物。其特点为:一般情况下,主要以晶体形式存在,具有较高的熔点和沸点,在熔融状态下或溶于水后其水溶液均能导电。为了解释这类化合物的键合情况,阐明结构和性质的关系,提出了离子键理论:
(1)当电负性小的活泼金属原子与电负性大的活泼非金属原子相遇时,它们都有达到稳定结构的倾向,由于两个原子的电负性相差较大,因此它们之间容易发生电子的得失而产生正、负离子。
(2)所谓稳定结构,对于主族元素来讲它们所生成的离子多数都具有稀有气体结构,即p轨道为全充满状态“如钠和氯原子相遇时,钠(3s1)失去一个电子而成带一个正电荷的钠离子Na+(2s22p6),氯(3p5)获得一个电子而成带一个负电荷的氯离子Cl–(3s23p6),而对于过渡元素来讲,生成的离子的d轨道一般都处于半充满的状态,但也有很多例外的情况。
(3)原子间发生电子的转移而形成具有稳定结构的正、负离子时,从能量的角度上看,一定会有能量的吸收和放出,而且新体系的能量一般也是最低的。以NaCl的势能曲线来看这一点,我们可以将NaCl的势能函数表示为:
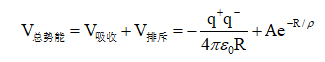
则势能曲线如图所示:

图1.NaCl势能曲线
由NaCl的势能曲线可知,当正、负离子相互接近时,在R较大时,由于电子云之间的排斥作用可忽略,这时主要表现为吸引作用,所以体系的能量随着R的减小而降低。当正负离子接近到小于平衡距离即R<R0,时,电子云之间的排斥作用上升为主要作用.这时体系的能量突然增大。只有当正、负离子接近平衡距离,即R =R0时。吸引作用与排斥作用才达到暂时的平衡,这时正、负离于处于平衡位置附近振动,体系的能量降到最低点。这说明正负离子之间,形成了稳定的化学键(即离子键)。
离子键的本质是静电作用力,是原子得失电子之后形成的正负离子通过静电吸引力形成的化学键,由于离子静电作用是球对称的,所以离子键没有方向性,也没有饱和性,但是由于离子半径的限制,会形成固定配位数的化合物,键的离子性与与元素的电负性有关,离子键形成的重要条件是相互作用的原子的电负性差值较大。一般元素的电负性差越大,它们之间键的离子性也就越大。小。对于AB型化合物单键离子性百分数和两原子电负性差值(χA–χB)之间的关系如图所示。

图2.单键的离子性与电负性差值之间的关系
由图可知,当两个原子电负性差值为1.7时,单键约具有50%的离子性,这是一个重要的参考数据。若两个原子电负性差值大于1.7时,可判断它们之间形成离子键,该物质是离子型化合物,如果两个原子电负性差值小于1.7,则可判断它们之间主要形成共价键,该物质为共价化合物。
离子具有以下三种特征:离子电荷,离子的电子层构型和离子半径。
从离子键的形成过程可知,正离子的电荷数就是相应原子失去的电子数,负离子的电荷数就是相应原子得到的电荷数,离子失去或得到的电子数,趋向于使原子结构达到更加稳定的状态,例如转变为稀有气体的结构,由此引出了离子的电子层构型,离子的电子层构型大致可以分为如下的种类:
①2电子构型:最外层为2个电子的离子,如Li+,Be2+等。
②8电子构型:最外层为8个电子的离子,如Na+,Cl– 等。
③18电子构型:最外层为18个电子的离子,如Cu+,Ag+等。
④(18+2)电子构型:次外层为18电子、最外层为2个电子的离子,如Pb2+和Sn2+等。
⑤8——17电子构型:最外层的电子为8——17之间的不饱和结构的离子,如Fe2+,Mn2+等。
离子的电子层构型同离子间的作用力,即同离子键的强度有密切的关系,一般来讲,在离子的电荷和半径大致相同的条件下,不同构型的正离子对同种负离子的结合力的大小可有如下经验规律:
8电子构型的离子<8-17电子构型的离子<18或18+2电子构型的离子
离子半径既可以由理论估算,也可以由实验测得,离子半径的变化规律是:
(a)在周期表各主族元素中,由于自上而下电子层数依次增多,所以具有相同电荷数的同族离子的半径依次增大,例如:

(b)在同一周期中主族元素随着族数递增,正离子的电荷数增大,离子半径依次减小。如:Na+>Mg2+>Al3+。
(c)若同一元素能形成几种不同电荷的正离子时,则高价离子的半径小于低价离子的半径。例如:
RFe3+(60pm)<RFe2+(75pm)
(d)负离子的半径较大,约为130—250pm,正离子的半径较小,约为10—170pm。
(e)周期表中处于相邻族的左上方和右下方斜对角线上的正离子半径近似相等。例如:
Li+(60pm)≈Mg2+(65pm)
由于离子半径是决定离子间引力大小的重要因素,因此离子半径的大小对离子化合物性质有显著影响。离子半径越小离子间的引力越大,要拆开它们所需的能量就越大,因此离子化合物的熔沸点也就越高。
离子晶体就是由正负离子经离子键作用而形成的晶体,具有多种结构,这里我们主要了解有关离子半径比对配位数和晶体构型的影响。
不同的正、负离子结合成离子晶体时,会形成配位数不同的空间构型,这是因为在某种结构下该离子化合物的晶体最稳定,体系的能量最低,一般决定离子晶体构型的主要因素有正、负离子的半径比的大小和离子的电子层构型等。这里以AB型的离子晶体举例,来看出离子半径比对配位数和晶体构型的影响。

图3.平面下正负离子可能的几何构型,其中黑色为正离子,白色为负离子
经过简单的几何计算可以得出以下结论:
即当r+/r-=0.414时,正、负离子间是直接接触的,负离子也是相互接触的。这种情况不能稳定存在。
当r+/r-=>0.414时,负离子之间接触不良,而正、负离子之间相互接触吸引作用较强。这种结构较为稳定,这是配位数为6的情况。但当r+/r-=>0.732时,考虑到三维空间中的几何构型,正离子相对地增大,它有可能接触更多的负离子,因此有可能使配位数成为8。
当r+/r-=<0.414时,负离子之间互相接触。而正、负离子之间接触不良,由于离子间排斥作用较大,这种结构不易稳定存在,故使晶体中离子的配位数降低.即配位数变为4。
根据这个简单的例子,我们可以明白对于离子晶体构型以及配位数的判断,在没有合成出相应的样品之前,通过目前的计算方法,我们也是可以得到一个最初的估计的,详细的数值模拟方法目前也是主流的研究方向。上述方法有几个需要注意的点:一是这种方法估计的构型并不是绝对的,例如在氯化铷中,Rb+离子与Cl–离子的半径比r+/r-≈0.82,理论上配位数应为8,实际上它为氯化钠型,配位数为6;二是外界条件的变化,离子的电子层构型,离子的数目,也都会对晶体构型产生影响,例如高压下,离子半径会相应的减小,也会造成晶体结构的变化;三是当离子半径比接近极限值0.414和0.732时,很有可能具有两种不同配位数的晶体构型。
2.共价键理论
离子键理论能很好地说明离子化合物的形成和特性。但它不能说明由相同原子组成的单质分子(如:H2,Cl2、N2等)的形成,也不能说明由化学性质相近的元素所组成的化合物分子(如HCl,H2O等)的形成。1916年美国化学家路易斯(G.N. Lewis)为了说明分子的形成,提出了共价键理论,他认为分子中每个原子应具有稳定的稀有气体原子的电子层结构。但这种稳定结构不是靠电子的转移,而是通过原子间共用一对或若干对电子来实现。这种分子中原子间通过共用电子对结合而成的化学键称为共价键。例如:

路易斯共价键理论虽能成功地解释了由相同原子组成的分子以及性质相近的不同原子组成的分子的形成,并初步揭示了共价键与离子键的区别。但是路易斯理论也有局限性,它不能解释为什么有些分子的中心原子最外层电子数虽然少于8或多于8,但这些分子仍能稳定存在,也不能解释共价键的特性(如方向性、饱和性)以及存在单电子键和氧分子具有磁性等问题。同时,它也不能阐明为什么”共用电子”就能使两个原子结合成分子的本质原因、直至1927年海特勒和伦敦把量子力学的成就应用于最简单的H2分子结构上,才使共价键的本质,获得初步的解答。后来,鲍利等人发展了这一成果,建立了现代价键理论(即电子配对理论)、杂化轨道理论、价层电子对互斥理论,1932年美国化学家密立根和德国化学家洪特提出了分子轨道理论。下面我们将简要地介绍这些理论。
价键理论
价键理论,又称电子配对法,简称VB法。它是海特勒和伦敦处理H2。问题所得结果的推广、它假定分子是由原子组成的,原子在未化合前含有未成对的电子,这些未成对的电子,如果自旋是相反的话,可以俩俩耦合构成”电子对”,每一对电子的耦合就形成一个共价键。这种方法与路易斯的电子配对法不同,它是以量子力学为基础的。
我们先来讨论氢分子的薛定谔方程的海特勒-伦敦解法

图4.氢分子的坐标
氢分子是含有两个氢分子核a及b和两个电子1和2的体系,它们之间的距离如图所示。这一体系的势能可以表示为(这里使用原子单位制,高斯单位制等适当的单位制,保证没用的系数全为1):

在玻恩-奥本海默近似下,氢分子的薛定谔方程为:

由于难以分离变量,也没有办法利用微扰法,1927年,海特勒和伦敦首先用变分法来求上述方程的解。假定基态氢分子是由两个基态氢原子组成的,第一个氢原子Ha1包含原子核a和电子1,第二个氢原子Hb2包含原子核b和电子2。如果两个基态氢原子之间没有相互作用,那么氢分子的波函数将是两个独立的氢原子的波函数的乘积,即

氢原子的基态波函数解为

若交换两个电子,氢分子波函数为

,但是由于全同性,两个波函数是等价的,不同之处在于交换了电子。这种由于交换电子而得到一组等价波函数的现象称为交换简并性。而当两个氢原子相互靠近,形成氢分子时,两个氢原子之间的相互作用不能忽略,这两个波函数都不能表示氢分子的状态,按照变分法的基本原理,我们可以把两个波函数的线性叠加
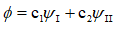
作为变分函数,变分函数的选择是带有尝试性的,选择的合理性要从计算结果和实验的契合程度来判断。
决定了变分函数的形式后,就可以利用变分法,求得c1,c2,两个近似波函数
ψS及ψA以及它们的近似能量ES和EA。计算结果如下:

其中,

详细计算过程较为复杂,这里直接给出最终的计算结果与实验数值之间的对比,如图所示:

图5.氢分子的能量曲线
从图中可以看出,与波函数ψS相对应的能量曲线ES有一个最低点,所以H2可以稳定的存在。两条能量曲线与实验测得的能量曲线近似,所以可以说明海特勒伦敦方法基本上是正确的,但是也可以比较明显的看出,这个方法得到的数值和实验相差还是较大的。与波函数ψA相应的能量曲线EA没有最低点,所以ψA的状态是不稳定的,它将自动的离解为两个氢原子。称ψS和ψA为基态和推斥态。如图为两种状态的电子云分布和等密度线:

图6.H2两种状态的电子云分布和等密度线(数字越大代表的密度越大)
由于电子具有自旋,且是一种费米子,所以空间部分波函数是交换对称的,自旋部分的波函数就是交换反对称的,空间部分的波函数是交换反对称的,自旋部分的波函数就是交换对称的,二电子体系的自旋部分的波函数为:

交换对称的自旋波函数,S取1,可以认为电子之间自旋平行,交换反对称的自旋波函数,S取0,可以认为电子之间自旋反平行。
至此,海特勒和伦敦处理氢分子问题的结果可以简述如下:当两个氢原子自远处接近(在远距离时有微弱的范德华引力)时,它们间的相互作用就渐渐增大。在较近的距离下,原子间的相互作用和它们的自旋有密切的关系。如果电子是反平行的,那么在到达平衡距离之前原子间的相互作用是吸引的,即体系的能量随R的减小而不断降低。在达到平衡距离以后,则体系的能量将随R的减小而迅速增高。因此 H2可以振动于平衡距离的左右而稳定地存在,这就是H2的基态。
综上,变分法对于H2的问题,虽然误差较大,但是结果的能量曲线和实验结果的对比,总体走向是完全没有问题的,且根据对自旋波函数的分析,可以看出这个导致这个结果的原因,主要来自于总自旋量子数的不同,或者说来自于自旋平行与反平行的不同,所以根据这个成功的理论计算,我们抽象出了价键理论的基本框架。
我们假定分子是由原子组成的,原子在未化合之前含有未成对电子,这些未成对的电子如果自旋是反平行的,可以两两耦合构成”电子对”。每一对电子的耦合就生成一个共价键。将理论推广到双原子分子和多原子分子时,要点如下:
(1)假定原子A和原子B各有一未成对电子且自旋相反,则可互相配对构成共价单键。如A和B各有两个或三个未成对电子,则能俩俩配对构成共价双键或三键,例如:
(i)Li-Li(锂蒸气的分子)是以单键结合的,因为Li原子虽然含有三个电子,但未成对的只有一个,所以只能构成共价单键。
(ii)N≡N分子是以三键结合的,因为N原子含有三个未成对电子,因此可以构成共价三键。
(iii)H—Cl是以单键结合的,因为H有一个未成对电子,Cl也有一个未成对电子,它们可以配对构成单键。
(iv)二个He原子互相接近时不能构成共价键,因为He原子没有未成对电子.
(2)如果A有二个未成对的电子,B只有一个,那么A就能和二个B化合成AB2分子,例如H2O。
(3)一个电子与另一个电子配对以后就不能再与第三个原子配对。例如二个H原子各有一未成对电子,它们能够配对构成 H2分子,如有第三个H 原子趋近 H2,就不能再化合成 H3分子,除非H2中的电子对被破坏以后,才能形成新的H2分子,如下式所示:
H+H-H→H-H+H
这种性质叫做共价键的饱和性。所谓饱和性,是指每个原子成键的总数或以单键联接的原子数目是一定的。这是因为共价键是由原子间轨道重叠和共用电子形成的,而每个原子能提供的轨道和成单电子数目是一定的。
(4)电子云最大重叠原理 :电子云的重叠愈多,所形成的共价键就愈稳固。在主量子数相同的原子轨道中,p轨道的电子云密集在它的对称轴的方向较s轨道更大,所以一般说来,p轨道形成的共价键较s轨道形成更为稳固。
根据电子云最大重叠原理,共价键的形成在可能范围内一定采取电子云密度大的方向,这就是共价键有方向性的根据。所谓共价键的方向性,是指一个原子与周围原子形成共价键有一定的角度。共价键具有方向性的原因是因为原子轨道(p,d,f)有一定的方向性,它和相邻原子的轨道重叠成键要满足最大重叠条件。
下图显示出氢的(1s)电子云与氯的(3p)电子云的三种重叠情况:(a)H沿z轴向Cl接近,结合而成稳固分子;(b)H沿另一方向向Cl接近,电子云重叠较少,结合不稳固,H有移向z轴的倾向;(c)H沿x轴向Cl接近,电子云没有重叠,因而且与Cl在这个方向不能结合。

图7.s和p电子云重叠的三种情况
了解了共价键的方向性和饱和性之后,我们可以简单讨论共价键的键型,这里主要讨论σ键和π键两种简单的共价键形式:
σ键的特点是:两个原子的成键轨道沿键轴的方向以“头碰头”的方式重叠;原子轨道重叠部分沿着键轴呈圆柱对称;由于成键轨道在轴向上重叠,故形成键时原子轨道发生最大程度的重叠,所以σ键的键能大、稳定性高。
π键的特点是:两个原子轨道以平行或“肩并肩”方式重叠;原子轨道重叠部分对通过一个键轴的平面具有镜面反对称性;从原子轨道重叠程度看,π轨道重叠程度要比σ键轨道重叠程度小,π键的键能要小于σ键的键能,所以π键的稳定性低于σ键,π键的电子活动性较高,它是化学反应的积极参加者。
(5)若原子A有孤对电子,原子B有能量合适的空轨道,原子A的孤对电子所占据的原子轨道和原子B的空轨道能有效地重叠,则原子A的孤对电子可以拿出来供原子A和B共享,这样形成的共价键称为共价配键,或简称配键,以符号A→B表示。原子A称为给电子体,原子B称为受电子体,箭头方向表示电子配给的方向。
(6)杂化轨道理论
价键理论比较简明地阐明了共价键的形成过程和本质,并成功地解释了共价键的方向性、饱和性等特点。但在解释分子的空间结构方面却遇到了一些困难。例如实验测定结果表明:甲烷分子的结构是一个正四面体结构,碳原子位于四面体的中心,四个氢原子占据四面体的四个顶点。CH4分子中形成四个稳定的C—H键,键角∠HCH为109°28‘,四个C一H键的强度相同,键能为411kJ·mol-1。
但是根据价键法,由于碳原子的电子层结构为1s22s22px12py1,只有两个未成对的电子,所以它只能与两个氢原子形成两个共价单键。如果考虑将碳原子的1个2s电子激发到2p轨道上去,则有四个成单电子(1个s电子和3个p电子),它可与四个氢原子的1s电子配对形成四个C—H键。由于碳原子的2s电子与2p电子的能量是不同的,那么这四个C—H 键应当不是等同的,这与实验事实不符,这是价键法不能解释的。为了解释多原子分子的空间结构,鲍利于1931年在价键法的基础上,提出了杂化轨道理论。
所谓杂化是指在形成分子时,由于原子的相互影响,若干不同类型能量相近的原子轨道混合起来,重新组合成一组新轨道。这种轨道重新组合的过程叫做杂化,所形成的新轨道就称为杂化轨道。杂化轨道与其它原子的原子轨道重叠形成化学键。例如CH4分子形成的大致过程示意如下:

图8.甲烷分子形成示意图
杂化轨道理论认为:在形成分子时,通常存在激发、杂化、轨道重叠等过程。但应注意,原子轨道的杂化,只有在形成分子的过程才会发生,而孤立的原子是不可能发生杂化的。同时只有能量相近的原子轨道(如2s,2p 等)才能发生杂化,而1s轨道与2p轨道由于能量相差较大,它们是不能发生杂化的。
下面来讨论几种常见的杂化形式:
sp杂化:sp杂化轨道是由一个ns轨道和一个np轨道组合而成的。它的特点是每个sp杂化轨道含有1/2s和1/2p的成分。sp杂化轨道间的夹角为180°,呈直线型。例如BeCl2(g)
sp²杂化:sp²杂化轨道是由一个ns轨道和两个np轨道组合而成的。它的特点是每个sp²杂化轨道都含有:1/3s和2/3 p的成分,杂化轨道间的夹角为120°,呈平面三角形。例如BF3。
sp³杂化:sp3杂化轨道是由一个 ns 轨道和三个np 轨道组合而成。它的特点是每个 sp3杂化轨道都含有1/4s和3/4p的成分,sp³杂化轨道间的夹角为109°28’,空间构型为四面体形。例如CH4。
sp3d²杂化:sp3d2杂化轨道是由一个 ns、三个 np 和二个nd 轨道组合而成。它的特点是六个sp3d²轨道指向正八面体的六个顶点,如图所示,sp3d2轨道间的夹角为90°或180°。例如SF6。

图9.sp3d2杂化轨道示意图
同种类型的杂化轨道又可以分为等性杂化和不等性杂化两种。最简单的不等性杂化的例子是水,按价键理论的观点,O原子有两个孤电子,和H原子化合之后的键角应该为90°,但实际上,键角104.5°,这个数值比较接近sp3杂化给出的109°28′,按杂化轨道理论解释,会存在两个孤电子对,所以可以判断出,孤电子对对杂化轨道,有排斥作用,这就是不等性的杂化轨道。
杂化轨道成键时,要满足原子轨道最大重叠原理,由于杂化轨道形成的电子云更加集中,所以杂化轨道的成键能力相比各原子轨道成键能力更强,形成的分子也更稳定,成键能力大小次序如下:

不等价杂化中孤电子对的排斥力更大,引出了后来的价层电子对互斥理论,这个理论主要通过计算孤电子对数,判断成键的形态,然后根据斥力的大小关系:孤电子对-孤电子对>孤电子对-成键电子>成键电子-成键电子。判断最终的空间构型,这里由于篇幅原因,不详细介绍这个方法。
分子轨道理论
价键理论认为形成共价键的电子只局限于两个相邻原子间的小区域内运动,缺乏对分子作为一个整体的全面考虑,因此它对有些多原子分子,特别是有机化合物分子的结构不能说明,同时它对氢分子离子H2+中的单电子键、氧分子中的三电子键以及分子的磁性等也无法解释。分子轨道理论(简称 MO法),着重于分子的整体性,它把分子作为一个整体来处理,比较全面地反映了分子内部电子的各种运动状态,它不仅能解释分子中存在的电子对键、单电子键、三电子键的形成,而且对多原子分子的结构也能给以比较好的说明。因此分子轨道理论在近些年来发展很快,在共价键理论中占有非常重要的地位。
下面,我们先介绍分子轨道理论的要点,然后针对双原子分子做一些简要的说明,多原子分子的分子轨道法较为复杂,这里不过多赘述。
分子轨道理论的要点:
(1)假设分子中每一个电子的运动状态可以用单电子波函数 ψσ来描写。单电子波函数的空间部分 ψ称为分子轨道,ψ2dr表示该电子在微体积dr内出现的几率,而ψ²则为几率密度(或称电子云密度),σ为自旋部分。
(2)分子轨道ψ可以近似地用原子轨道的线性组合(缩写为LCAO)表示,组合系数可用变分法或其他方法确定。用LCAO表示分子轨道的方法叫做原子轨道线性组合的分子轨道法(缩写为LCAO ,MO)。
(3)假设每一分子轨道 ψi:有一相应的能量 Ei,Ei近似地表示处于该分子轨道上的电子的电离能(库普曼斯定理)。分子中的电子按照泡利原理和最低能量原理排布在诸分子轨道上。
(4)为了有效地组成分子轨道,参与组成该分子轨道的原子轨道必须满足:(i)能量相近条件;(ii)对称性匹配条件;(iii)轨道最大重叠条件。
理论计算较为复杂,这里简要说明:
分子轨道为两个原子轨道的线性组合,即 带入薛定谔方程,解久期方程,可以得到能量的表达式,若将
带入薛定谔方程,解久期方程,可以得到能量的表达式,若将 忽略不计,
忽略不计, ,
, ,可以得到分子轨道的能量EI,EII的值为:
,可以得到分子轨道的能量EI,EII的值为:

因为B>0,所以 ,该式说明,两个原子轨道的线性组合得到两个分子轨道,其中一个是成键分子轨道,其能量比原子轨道中能量较低的轨道的能量还低;另一个是反键轨道,其能量比两个原子轨道中能量较高的轨道的能量还要高。分子轨道与原子轨道的能量关系如示。
,该式说明,两个原子轨道的线性组合得到两个分子轨道,其中一个是成键分子轨道,其能量比原子轨道中能量较低的轨道的能量还低;另一个是反键轨道,其能量比两个原子轨道中能量较高的轨道的能量还要高。分子轨道与原子轨道的能量关系如示。

图10.能量不同的原子轨道组成分子轨道时的近似能量关系
根据计算过程,我们可以看出,当E1和E2差距过大时,分子轨道的能量分别就是原子轨道的能量,相当于这两个原子轨道之间没有耦合,不能有效形成分子轨道,这一条件称为能量近似条件。H12绝对值越大,成键分子的能量降低越多。该数值与重叠积分S12相近,所以为了有效的组成分子轨道,参与成键的两个原子轨道重叠越多越好,这一条件常称为轨道最大重叠条件。最后,从群论的角度,原子轨道只有对称性相匹配,才能有效组成分子轨道,这一条件被称为对称性条件。
下面我们来讨论分子轨道理论对σ键和π键的解释,以及简要说明分子轨道理论较价键理论的优点在哪里。
σ轨道和σ键
σ键的形成和σ轨道如图所示

图11.σg1s轨道和σu*1s轨道

图12.σg2p轨道和σu*2p轨道
g和u分别表示德文中的偶的(gerade)和奇的(ungerade),来表示分子轨道是否具有中心对称性。从量子力学的计算中我们知道,这两个分子轨道沿轴的分量等于0,这种轨道被定义为σ轨道,用于和价键理论相对应。
π轨道和π键
π键的形成和π轨道如图所示
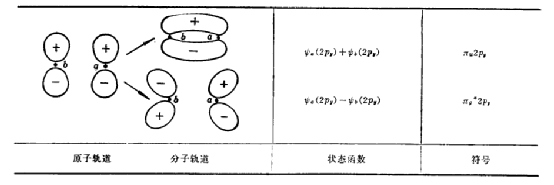
图13.πg2py轨道和πu*2py轨道
根据量子力学计算,分子轨道在键轴上的投影为+1或-1,2py和2px是线性组合之后的轨道。将投影为+1或-1的轨道称为π轨道。
这里以氧分子的能级示意图简要说明分子轨道理论

图14.氧分子轨道能级图
根据上述的理论要点,氧分子一共有16个电子,每个分子轨道可以容纳两个电子,所以从低到高之后,氧分子的分子轨道排布为:
O2[KK(σg2s)2(σu*2s)2(σg2p)2(πu2px)2(πu2py)2(πg*2px)1(πg*2px)1]
可以看出,氧分子有两个单电子,自旋角动量为1,是一个顺磁性分子,这是符合实验的,而价键理论认为,任何基态分子都应该为自旋单重态,也就是S=0,也就无法解释更加复杂的物理现象。
分子轨道理论精确,但是对于多原子体系来说,较为复杂,价键理论虽然有部分物理现象无法解释,但是对分子构型的判断上,以及对大概的物理性质的解释都是比较符合实际的,所以两种理论都应该得到重视,在物理研究中都应该有所了解。
参考文献
1.章慧. 卢嘉锡, 徐光宪《物质结构》[J]. 大学化学, 2021, 36(4): 2102048-0.
2.宋天佑, 程鹏, 王杏乔, 等. 无机化学 (上册)[J]. 教 育 出 版 社, 2004.
3.Roothaan C C J. New developments in molecular orbital theory[J]. Reviews of modern physics, 1951, 23(2): 69.
4.Gauld J W. Reviews in Computational Chemistry, Volume 20 [J]. 2005.
5.Heitler W, London F. Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik[J]. Zeitschrift für Physik, 1927, 44(6): 455-472.










暂无评论内容